گامهای مهندسی ژنتیکی برای تحقق رویای افزایش طول عمر


به گزارش ایران اکونومیست، همه ما برای داشتن زندگی طولانی و سالم تلاش میکنیم اما آیا واقعا امکان افزایش دادن طول عمر وجود دارد؟ «مؤسسه ملی بهداشت آمریکا»(NIH) میگوید که بهترین راه برای افزایش دادن طول عمر، خوب غذا خوردن، داشتن خواب باکیفیت، ورزش منظم، معاینات پزشکی منظم و اجتناب کردن از عادتهای بد مانند سیگار کشیدن و نوشیدن الکل است.
عملکرد یک ژن میتواند تأثیرات مهمی را بر طول عمر یک موجود داشته باشد. ممکن است باور کردن این موضوع دشوار به نظر برسد زیرا عوامل بسیاری از جمله مجموعهای از عوامل سبک زندگی و فهرست طولانی از بیماریها در تعیین کردن طول عمر نقش دارند. با وجود این، زمانی که ژنهای خاصی از توالی ژنتیکی حذف میشوند، اثرات قابل توجهی را بر طول عمر میگذارند. علاوه بر این، پژوهشهای گوناگون به ویژه پژوهشهایی که در مورد کرمهای لولهای میکروسکوپی انجام شدهاند، همچنان سرنخهای وسوسهانگیزی را در مورد مسیرهای مولکولی دخیل در پیری در اختیار دانشمندان قرار میدهند.
دانشمندان هنگام مطالعه کردن طول عمر تمایل دارند با موجوداتی کار کنند که عمر زیادی ندارند. بدین ترتیب، آنها میتوانند کل مسیر وجود داشتن یک ارگانیسم را مشاهده کنند و نتایج تجربی نسبتا سریعی را به دست بیاورند. یکی از ارگانیسمهایی که پژوهشگران اغلب در مطالعات خود پیرامون طول عمر از آن استفاده میکنند، یک کرم لولهای میکروسکوپی موسوم به «کرم الگانس»(C. elegans) است که معمولا بین دو تا سه هفته زندگی میکند. مزیت دیگر استفاده کردن از کرمهای الگانس این است که آنها فیزیولوژی سادهای دارند و میتوان ژنهای آنها را به سادگی دستکاری کرد.
دانشمندانی که برای کند کردن روند پیری تلاش میکنند، طول عمر کرمها، موشها و حتی میمونها را تا حدودی افزایش دادهاند اما آیا آنها میتوانند همین کار را برای انسانها انجام دهند؟
تنظیم ژنتیکی مجدد برای افزایش دادن طول عمر
گروهی از دانشمندان «دانشگاه کالیفرنیا سندیهگو»(UC San Diego) در آوریل سال ۲۰۲۳ یک پژوهش را در مورد افزایش طول عمر با تنظیم ژنتیکی مجدد منتشر کردند. آنها موفق شدند با دستکاری مدار ژنتیکی که پیری را کنترل میکند، طول عمر یک موجود ساده را تا حدود ۸۰ درصد افزایش دهند.
آنها چندین سال است که پیری سلولی را مطالعه میکنند و در این پژوهش دریافتند که سلولها در طول زندگی خود، زنجیرهای از تغییرات مولکولی را دنبال میکنند تا این که در نهایت تحلیل میروند و میمیرند. با وجود این، همه سلولها به یک شکل پیر نمیشوند و این تمرکز آنها در پژوهش جدید بود.
آنها ابتدا از شبیهسازی رایانهای پیری سلولی برای آزمایش کردن ایدههای خود استفاده کردند و سپس، به اصلاح مدارهای پیری در مخمر تکسلولی «ساکارومایسس سرویزیه»(Saccharomyces cerevisiae) پرداختند.
سلولها در طول زندگی خود، زنجیرهای از تغییرات مولکولی را دنبال میکنند تا این که در نهایت تحلیل میروند و میمیرند. با وجود این، همه سلولها به یک شکل پیر نمیشوند.این گروه پژوهشی دریافتند که سلولها یکی از دو مسیر پیری را دنبال کردهاند. حدود نیمی از سلولها به کاهش تدریجی پایداری DNA یا «پیری هستهای» دچار شدند. برای بقیه سلولها، مسیر پیری با کاهش یافتن منبع مطمئن میتوکندری آنها مشخص شد که اندامکهایی برای تامین انرژی سلول هستند. این روند، «پیری میتوکندری» نامیده میشود.
پژوهشگران برای کنترل پیری سلولها، بیان دو مولکول تنظیمکننده رونویسی را دستکاری کردند که تعیین میکنند کدام ژنها در سلول فعال هستند. مولکول «Sir2» باعث پیری هستهای میشود که بیثباتی DNA را به دنبال دارد و مولکول «Hap4» با فعالیت میتوکندری مرتبط است.
وقتی یکی از این تنظیمکنندهها بیان میشود و به فعالیت میپردازد، از بیان شدن دیگری جلوگیری میکند. بنابراین پژوهشگران، یک نوسانساز ژن مصنوعی را برای تنظیم مجدد این مکانیسم مهندسی کردند. پژوهشگران با ایجاد نوسانات پایدار در سلولها، پیروی سلولها از هر یک از دو مسیر پیری را متوقف کردند. در نتیجه، طول عمر این سلولها افزایش یافت.
پروفسور «نان هائو»(Nan Hao) یکی از مدیران «مؤسسه زیست شناسی مصنوعی»(Synthetic Biology Institute) در «دانشگاه کالیفرنیا سندیگو»(UC San Diego) و پژوهشگر ارشد این پروژه گفت: پژوهش ما یک اثبات مفهوم است و نشان میدهد همان طور که مهندسان مکانیک میتوانند خودروهای ما را تعمیر کنند و ارتقا دهند تا بیشتر دوام بیاورند، ما نیز میتوانیم از همین روش مهندسی برای اصلاح و تقویت کردن سلولهای خود و داشتن زندگی طولانیتر استفاده کنیم. نکته برجسته این پژوهش، روش ما برای دستیابی به هدف است. ما از رایانه برای شبیهسازی کردن سیستم پیری طبیعی و طراحی و مهندسی منطقی سیستم برای افزایش طول عمر استفاده میکنیم.
دانشمندان با ایجاد نوسانساز ژن، به تبادل مداوم سلولهای مخمر بین دو مسیر پیری پرداختند و از انحراف آنها به مسیر از پیش تعیینشده خود یعنی زوال و مرگ جلوگیری کردند و روند انحطاط سلولها را کاهش دادند.

سلولهای مخمری که به طور مصنوعی دوباره تنظیم شدند و با هدایت نوسانساز مصنوعی به سوی پیری رفتند، در مقایسه با سلولهای کنترلشده، ۸۲ درصد افزایش طول عمر داشتند. هائو گفت: به نظر نمیرسد که دستکاری ژنتیکی بر آنها تأثیر منفی بگذارد زیرا سلولهای مخمر به خوبی و با سرعت رشد بالا زنده میمانند.
هائو ادامه داد: این اولین بار است که یک روش مبتنی بر مهندسی محاسباتی در تحقیقات پیری مورد استفاده قرار میگیرد. من نمیتوانم بفهمم که چرا ما نمیتوانیم همین راهبرد را روی سلولهای انسانی اعمال کنیم. همه سلولها حاوی مدارهای تنظیمکننده ژن هستند که مسئولیت بسیاری از عملکردهای فیزیولوژیکی از جمله پیری را بر عهده دارند. بنابراین از نظر تئوری، این روش میتواند در سلولهای انسانی کارآیی داشته باشد.
هدف این پژوهش نه تنها میتواند افزایش عمر موجودات پیچیدهتر باشد، بلکه ممکن است بتوان از آن برای افزایش عمر برخی از سلولهای بدن موجودات به منظور جلوگیری کردن از بیماریهای دژنراتیو استفاده کرد.
با وجود این، هائو هشدار داد که آنها نمیدانند آیا افزایش طول عمر ممکن است به روشهای دیگری هم روی سلولها تأثیر بگذارد یا خیر. هائو خاطرنشان کرد: این یک پرسش بیولوژیکی عمیق است. فرضیه کنونی ما این است که طول عمر سلول، یک صفت انتخابشده از طریق تکامل نیست. سلولها ابتدا باید بتوانند در محیط استرسزا که به سرعت در حال تغییر کردن و غیر قابل پیشبینی است، زنده بمانند.
وی افزود: این احتمال وجود دارد که سلولهای مهندسیشده دارای عمر طولانی، در برابر انواع خاصی از تنشهای محیطی مقاومت کمتری داشته باشند. بنابراین، اساسا افزایش طول عمر شاید برخی از عملکردهای عادی را قربانی کند اما این فقط یک فرضیه است.
هائو باور دارد که ممکن است پتانسیلی برای به کار گرفتن این روش در انسان وجود داشته باشد. هر دو تنظیمکننده در بدن انسان هم وجود دارند. بنابراین، شاید بتوان همین راهبرد را برای سلولهای انسانی به کار برد.
پروفسور «هاوارد سالیس»(Howard Salis) پژوهشگر ارشد «آزمایشگاه سالیس»(Salis Lab) در «دانشگاه ایالتی پنسیلوانیا»(Penn State) که در این پژوهش شرکت نداشت، گفت: اگر هدف جمعی این مداخلات، حفظ کردن وضعیت سلولی سالمتر باشد، پس خطرات و عوارض بیماریهای مرتبط با سن کاهش مییابد.
این پژوهش در مجله «Science» به چاپ رسید.
افزایش طول عمر تا ۱۲۰ سال
اگر روزی به شما گفته شود که میتوانید طول عمر خود را چه از نظر ذهنی و چه از نظر جسمی افزایش دهید، چه واکنشی خواهید داشت؟
پژوهشگران «دانشگاه ویرجینیا»(UVA) در مارس سال ۲۰۲۳، افزایش طول عمر سالم با درصد چشمگیر را در دو مدل بیولوژیکی شامل مخمرها و کرمهای لولهای گزارش دادند. همچنین، آنها گزارش دادند که مدرکی دال بر همین فرآیند ترمیم در انسانها پیدا کردهاند. پژوهشگران باور دارند ژنی که آنها شناسایی کردهاند، از طریق حذف کردن محصولات جانبی سمی چربی، پیری را کنترل میکند. آنها این فرآیند را «AMAR» می نامند.
فرآیند AMAR به مجموعه رو به رشد تحقیقات ضد پیری میپیوندد. اطلاعات و نوآوریهای جدید به صورت روزانه وارد میشوند. به نظر میرسد پیری در راه تبدیل شدن به یک موضوع قابل مذاکره است. اکنون به نظر میرسد سوال این نیست که آیا درمانهای ضد پیری وجود خواهند داشت یا خیر، بلکه موضوع این است که چه زمانی درمانهای ضد پیری ارائه خواهند شد.
با گذشت زمان، ما پیر میشویم اما بدن و ژنهای ما این ظرفیت را دارند که فرآیند پیری را سرعت ببخشند یا کند کنند.«آیلین اورورک»(Eyleen O’Rourke) دانشیار و عضو «مرکز تحقیقات قلب و عروق رابرت ام. برن»(CVRC) گفت: زمانی این تصور در جامعه علمی وجود داشت و هنوز هم بین عموم مردم این تصور وجود دارد که پیری یک روند اجتنابناپذیر است. با گذشت زمان، ما پیر میشویم اما بدن و ژنهای ما این ظرفیت را دارند که این فرآیند را سرعت ببخشند یا کند کنند.
دانشمندان بیش از یک دهه است که میدانند چندین مسیر ژنتیکی و بیوشیمیایی میتوانند عمر یک شخص را افزایش یا کاهش دهند. اورورک گفت که پاسخ دادن به دلیل تکامل ژنوم به این شکل پیچیده است اما تلاش برای ارائه دادن یک پاسخ کوتاه ادامه دارد.
بدن ما یک شبکه ارتباطی پیچیده ای است. اورورک و همکارانش، ورودیها و پیوندهای میانی مرتبط با پیری را پیش از آغاز پژوهش خود شناسایی کردند و با توجه به اطلاعات بهدستآمده توسط دانشمندان پیشین، راههایی را برای کاهش سرعت و حتی معکوس کردن پیری در حیواناتی مانند موشهای آزمایشگاهی یافتند.
اورورک توضیح داد: مشکل کار کردن با بسیاری از ژنهای ورودی و پیوندهای میانی این است که چون آنها بازیگران مهمی در سلول هستند و چیزهای زیادی را کنترل میکنند، یافتن یک وضعیت در سلول بسیار دشوار یا حتی غیر ممکن است و فقط میتوان اثرات خوب تغییر فعالیتهای آنها را دریافت کرد.
کرمها به طور سنتی همیشه با مرگ مرتبط بودهاند اما در علم، کرمها به ویژه کرمهای لولهای، مسئول برخی از پیشرفتهای مهم پزشکی بودهاند که برنده جوایز نوبل در این حوزه شدهاند.
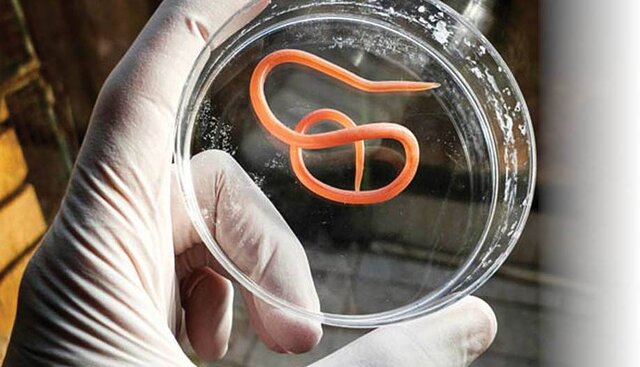
اورورک و همکارانش از کرم الگانس استفاده کردند که بدن شفافی دارد و اولین ارگانیسم چندسلولی به شمار میرود که کل ژنوم آن توالییابی شد. شاید این کرم دور از ما انسانها به نظر برسد اما مسیرهای شیمیایی آن به طور قابلتوجهی مشابه هستند. گروه با استفاده از کرم الگانس به عنوان یک مدل کلیدی برای این پژوهش، به دنبال رمزگشایی چیزی بودند که در انتهای زنجیرههای ارتباطی پیشین کنترل کننده پیری روی میدهد.
اورورک به طور ویژه میخواست بازیگران مولکولی را پیدا کند که مسئول پیری هستند؛ یعنی سلولهایی که سلولها را در هم میشکنند یا ترمیم میکنند و در نتیجه، بافتها و اندامها را بهبود میبخشند. تصور این بود که با قرار گرفتن در انتهای زنجیره ارتباطی، بازی با ژنها ممکن است به معنای بروز اثرات ناخواسته کمتری باشد.
پژوهشگران با بررسی فرآیند طبیعی پاکسازی و ترمیم سلولی در زیستشناسی که «اتوفاژی»(Autophagy) نام دارد، کار خود را آغاز کردند. مدتها تصور میشد که دستور ترمیم سلولها، زیربنای طول عمر است. اورورک گفت: اتوفاژی فرآیندی است که قسمتهای ناخواسته سلولها را پاکسازی و بازیافت میکند. وقتی اجزای سلول خراب میشوند، باید آنها را دور ریخت. بدین منظور، اتوفاژی سلولها را تجزیه میکند تا قطعات آنها را برای ساخت اجزای سلولی جدید به کار ببرد. بنابراین، اتوفاژی گزینه اصلی ضد پیری بود.
اگر فرضیه آنها درست بود و اتوفاژی باعث افزایش طول عمر میشد، با متوقف کردن آن، حیوانات بیشتر عمر نمیکردند. اورورک ادامه داد: اما این اتفاق نیفتاد. ما اتوفاژی را به روشهای گوناگون -از نظر ژنتیکی، با مواد شیمیایی و همه روشهای کاملا ثابتشده- غیرفعال کردیم و توانستیم تأیید کنیم که اتوفاژی غیرفعال شده است اما حیوانات به زندگی سالم طولانی ادامه دادند. این همان زمانی بود که ما جستجوی یکباره را از طریق صدها ژن آغاز کردیم تا بتوانیم دلیل واقعی طول عمر را پیدا کنیم.
این پژوهش، آنزیمی را معرفی کرد که الکل را در بدن انسان تجزیه میکند و میزان سمی بودن آن را در بدن کاهش میدهد. در واقع، پزشکان این آنزیم را هدف قرار میدهند تا به الکلیها کمک کنند که سلولهای خود را پس از سالها سوءمصرف الکل تمیز کنند. نام آنزیم «ADH-1» است و ژن تولیدکننده آنزیم «adh-1» نام دارد.
اگرچه علتهای مرگ اغلب به مقولههایی مانند سالمندی طبقهبندی میشوند اما دلایل مرگومیر پیچیده هستند و تنوع آنها تقریبا به اندازه تنوع خود بشر است.سپس پژوهشگران، آزمایش ژن adh-1 را برای کاهش یا افزایش دادن سرعت تولید آنزیم آغاز کردند. آنها ژن را در کرمها از دو روش تقویت کردند. سپس با استفاده از یک سوزن کوچک، چندین نسخه از ژن را به بدن یک کرم لولهای باردار انتقال دادند. همچنین، پژوهشگران کرمها را از طریق ویرایش ژن کریسپر اصلاح کردند تا نسخهای از adh-1 را بیان کند که در تاریکی میدرخشد.
در همین حال، آزمایشگاه ژنتیک مولکولی «جفری اسمیت»(Jeffrey Smith) از روشهای ژنتیکی مشابه برای بیشفعال کردن ژن مشابه موجود در مخمر نانوایی استفاده کردند. آنها نشان دادند که افزایش طول عمر فقط همین یک بار در کرم لولهای نیست. اسمیت نتیجه گرفت: بیان بیش از اندازه به تنهایی برای افزایش طول عمر کافی بود.
اصلاح ژنتیکی کرمها، به زنده ماندن تا چند هفته بیشتر محدود نشد، بلکه کرمها انواع مزایا را دریافت کردند. اورورک گفت: تاکنون اثرات مثبتی را در سراسر جهان از نظر افزایش قدرت عضلانی، کاهش ذخیره چربی، افزایش حافظه و یادگیری و همچنین افزایش طول عمر مشاهده کردهایم.
بر کسی پوشیده نیست که انسان با رژیم غذایی مناسب و ورزشهای روزمره، همراه با مراقبت از خود مانند کاهش استرس و خواب کافی میتواند عمر طولانیتری داشته باشد. با وجود این، بیشتر مردم پیش از این که سن آنها به ۸۰ برسد، از دنیا میروند. اگرچه علتهای مرگ اغلب به مقولههایی مانند سالمندی طبقهبندی میشوند اما دلایل مرگومیر پیچیده هستند و تنوع آنها تقریبا به اندازه تنوع خود بشر است.
اما یکی از دلایل مشترک، ذخایر چربی است که adh-1 روی آنها کار میکند. مدتهاست که مشخص شده کاهش دادن کالری به افزایش طول عمر میانجامد. این در حالی است که چاقی مرگ را سرعت می بخشد. اعضای آزمایشگاه اورورک پیشتر مجموعهای از ژنهای مرتبط با چاقی را شناسایی کردهاند. این مجموعه شامل ۱۴ ژن است که باعث افزایش وزن میشوند و سه ژن که میتوانند از افزایش وزن جلوگیری کنند.
این پژوهش در مجله «Current Biology» به چاپ رسید.
ژنهای پرشکننده
همه متخصصان ژنتیکی میگویند که ژنوم ما میتواند یک مکان آشفته باشد زیرا DNA ما علاوه بر داشتن دستورالعملهای لازم برای زندگی، مجموعهای از قطعات ژنتیکی متحرک را نیز در خود جای میدهد که میتوانند خودبهخود جان بگیرند، خود را کپی کنند، به درون و بیرون DNA منتقل شوند و ژنهای ما را تخریب کنند. این عناصر که «ترانسپوزونها»(Transposons) یا «ژنهای پرشکننده»(Jumping Genes) نامیده میشوند، مانند ارواح متحرک DNA به نظر میرسند. گاهی اوقات آنها خود را به ژنهای ضروری وارد میکنند اما قرار دادن آنها به صورت اشتباه میتواند به بروز سرطان، بیماری و مرگ سلولی منجر شود. علاوه بر این، تعداد زیادی از آنها وجود دارند و دانشمندان تخمین میزنند که تقریبا نیمی از DNA ما ترانسپوزون است.
تنها دلیلی که سلولهای ما میتوانند بدون تسلیم شدن در برابر هرجومرج و آسیب این غارتگران متحرک کار کنند، این است که ژنوم میتواند آنها را خاموش کند. در بیشتر مدت زندگی بزرگسالان، این عناصر در کروموزومها محبوس هستند و به ناحیهای به شدت آسیبدیده و غیر قابل دسترس به نام «هتروکروماتین» متصل شدهاند. به لطف این مکانیسم، سرطان نسبتا غیر رایج باقی میماند و سلولهای ما در بیشتر مدت عمر ما بدون مشکل کار میکنند.
در چند سال گذشته، دانشمندان دریافتهاند که ترانسپوزونها لزوما ساکت نمیمانند. در آزمایشهایی که روی مخمر، مگس میوه، موشها و حتی انسانها انجام شد، آنها افزایش فعالیتهایی را مشاهده کردند که با افزایش سن به وجود میآیند. «جان سدیوی»(John Sedivy) زیستشناس «دانشگاه براون»(Brown University) گفت: طی ۱۰ سال گذشته، این امر به عنوان روندی که در طول پیری طبیعی اتفاق میافتد، تثبیت شده است. هیچ کس هنوز آزمایشی را انجام نداده است که نشان دهد اگر از این امر جلوگیری کنیم، چه اتفاقی رخ میدهد و آیا روی پیری تأثیر میگذارد.
این پژوهش جدید، پژوهشگران را یک گام به نشان دادن این ارتباط نزدیکتر میکند. پژوهشگران مجارستانی، چندین خانواده از ترانسپوزونها را در کرم الگانس خاموش کردند و افزایش قابل توجه طول عمر را نشان دادند.
کرم لولهای یک ژنوم فشرده دارد که بخش کوچکی از آن ترانسپوزون است. پژوهشگران نشان دادند که کدام خانواده ترانسپوزون با افزایش سن فعالتر شدند. سپس، آنها سیستمهای مولکولی جدیدی را برای مسدود کردن آنها توسعه دادند. مسدود کردن چندین ژن به طور همزمان، یک چالش فنی مهم را ایجاد میکند زیرا بسیاری از این سیستمها به صورت همزمان تنها یک ژن را هدف قرار میدهند.
مسدود کردن ترانسپوزونها به افزایش طول عمر قابل توجه بین یک تا چهار روز انجامید. میانگین طول عمر کرمها حدود ۲۱ روز است. بنابراین، این نتیجه افزایش پنج تا ۱۵ درصدی را نشان میدهد. هنگامی که پژوهشگران بیش از یک خانواده ترانسپوزون را به صورت همزمان مسدود کردند، یک اثر افزایشی مشاهده شد که روزهای ارزشمندتری را به کرمهای کوچک اعطا کرد.
«تیبور ولای»(Tibor Vellai) پژوهشگر متخصص پیری در «دانشگاه اوتووش لوراند»(ELTE) در مجارستان و پژوهشگر ارشد این پروژه گفت: این یک مداخله بزرگ بود. این پژوهش نشان میدهد که پیری توسط عوامل ژنتیکی تنظیم میشود، نه فقط به صورت تصادفی.
این پژوهش در مجله «Nature Communications» به چاپ رسید.
جستوجوی ژن افزایش طول عمر
سگهای «گلدن ریتریور»(Golden Retriever) یکی از محبوبترین نژادهای سگ هستند اما پژوهشها نشان میدهند که آنها تا ۶۵ درصد در معرض مرگ بر اثر سرطان قرار دارند. پژوهشگران «دانشگاه کالیفرنیا دیویس»(UC Davis) تصمیم گرفتند تا بفهمند که آیا برخی از عوامل ژنتیکی میتوانند به میزان بقای سگهای گلدن ریتریور کمک کنند اما به جای جستوجوی ژنهای مرتبط با تشخیص سرطان در این نژاد، آنها به دنبال ژنهای مرتبط با طول عمر بیشتر بودند.
ژنی که آنها پیدا کردند، در خانوادهای از پروتئینها وجود دارد که مدتهاست نقش آنها در سرطانهای انسانی مهم شناخته شده است. نسخهها یا انواع خاصی از ژن با افزایش طول عمر تا حدود دو سال مرتبط بودند.
«رابرت ربهون»(Robert Rebhun) رئیس بخش انکولوژی در دانشکده دامپزشکی کالیفرنیا دیویس گفت: فرضیه ما این است که بیشتر سگهای گلدن رتریور، استعداد ژنتیکی را برای سرطان دارند اما اگر برخی از آنها تا ۱۴، ۱۵ یا ۱۶ سالگی زندگی میکنند، احتمالا باید یک عامل ژنتیکی دیگر وجود داشته باشد که به کاهش ژنهای بد کمک میکند و ژنی که برای ما ظاهر شد، «HER4» است.
ژن HER4 که با نام «ERBB4» نیز شناخته میشود، عضوی از خانواده گیرندههای فاکتور رشد اپیدرمی انسانی است. این همان خانواده ژن HER2 در انسان است که به رشد سریع سلولهای سرطانی کمک میکند. ربهون گفت: سگها به انواع سرطانهای مشابه سرطانهای انسان مبتلا میشوند که میتواند این کشف را برای انسانها نیز مهم کند.
وی افزود: اگر متوجه شویم که این نوع از HER4 برای شکلگیری یا پیشروی سرطان در سگهای گلدن رتریور نیز مهم است یا واقعا میتواند خطر ابتلا به سرطان را در این جمعیت مستعد سرطان تغییر دهد، میتوان از آن در پژوهشهای آینده سرطان انسان استفاده کرد.
این پژوهش در مجله «GeroScience» به چاپ رسید.
ارائه درمانهای ضد پیری در دهه آینده
دانشمندان در آستانه برطرف کردن پیری هستند و بر این باورند که ممکن است درمانهایی برای کاهش تأثیر آن در دهه آینده وجود داشته باشند. گروهی از پژوهشگران «دانشگاه کمبریج»(University of Cambridge) باور دارند پاسخ در فیلها، نهنگها و عروس دریایی نامیرا نهفته است که طول عمر بیشتری دارند و در برابر سرطان مقاوم هستند. به نظر میرسد کلید طول عمر این موجودات، توانایی ترمیم کردن آسیبهای موجود در DNA آنها باشد.
این گروه پژوهشی اکنون در تلاش هستند تا این تواناییها را به انسان منتقل کنند. این تواناییها سلولها را به حالت عملکردی جوانتر بازمیگردانند تا ظهور همه بیماریهای مرتبط با افزایش سن را به تاخیر بیندازند.
آسیبهای DNA در بدن ما جمع میشوند زیرا ما به صورت روزمره در معرض عوامل آسیبرسان مانند اشعه فرابنفش خورشید، آلایندههای ناشی از اگزوز خودروها و صنایع و حتی مواد غذایی سوختهشده قرار می گیریم.
به گفته پژوهشگرانی که این حیوانات را مطالعه کردهاند، ترمیم DNA میتواند از تجمع جهشهای ژنتیکی عامل بیماری و مرگ در سنین بالا جلوگیری کند. «دلفین لاریو»(Delphine Larrieu) از پژوهشگران این پروژه گفت: زمان بسیار هیجانانگیزی برای پژوهش در مورد پیری است. من معتقدم که در دهه آینده شاهد ظهور مداخلات ضد پیری انسان خواهیم بود.
ترمیم DNA میتواند از تجمع جهشهای ژنتیکی عامل بیماری و مرگ در سنین بالا جلوگیری کند.دو نمونه از موجوداتی که پژوهشگران در آنها به دنبال راهبرد میگردند، بزرگترین پستانداران –فیلها و نهنگها- هستند. هر دو پستاندار دارای ژنهای منحصربهفردی هستند که با مقاومت در برابر سرطان و ترمیم آسیب DNA ارتباط دارند. انسانها نیز دارای ژنی به نام «p۵۳» هستند اما تعداد آنها بسیار کمتر است و فقط دو نسخه را در مقایسه با ۲۰ ژن فیل شامل میشود.
دانشمندان معتقدند به همین دلیل است که با وجود جثه بزرگ فیلها، میزان مرگومیر ناشی از سرطان در آنها حدود ۴.۸ درصد برآورد میشود. این عدد در انسانها بین ۱۱ تا ۲۵ درصد است. نهنگها ۲.۴ برابر بیشتر دارای ژنهای سرکوبکننده تومور هستند.
اگر نهنگها در هر سلول همان خطر سرطان را داشتند که انسانها دارند، این خطر در چهار میلیارد سلول آنها ضرب میشد و این موجودات هرگز به اولین تولد خود نمیرسیدند.
دکتر «الکس کیگان»(Alex Cagan) پژوهشگر دپارتمان ژنتیک دانشگاه کمبریج گفت: این نشان میدهد که نهنگها باید مکانیسمهای بهتری را نسبت به انسان برای مقاومت کردن در برابر سرطان داشته باشند. این امکان وجود دارد که هر کاری آنها برای مقاومت در برابر پیری انجام میدهند، همان چیزی است که آنها را کمتر در معرض ابتلا به سرطان قرار میدهد. برخی از این موجودات میتوانند تا ۲۰۰ سال عمر کنند. اگر جهش DNA به پیری و سرطان منجر شود، کاهش میزان جهش با داشتن واکنشهای دقیقتر به آسیب DNA ممکن است بتواند هر دو مشکل را به طور همزمان حل کند.
پاسخ، ژنهای سرکوبگر تومور نیست، بلکه ترمیم مستقیم آسیب DNA در نهنگ قطبی است که میتواند بیش از ۲۰۰ سال زندگی کند.
اگرچه این پستانداران میتوانند کلید درمان بیماریهای مرتبط با افزایش سن باشند اما عروس دریایی نامیرا میتواند روند پیری را کاملا کند کند. به گفته پژوهشگرانی که ژنوم عروس دریایی نامیرا را مورد بررسی قرار دادند، این موجود با سایر عروسهای دریایی تفاوت دارد و تنها نوعی است که در مراحل پس از تولید مثل، پتانسیل جوانسازی خود را تا ۱۰۰ درصد حفظ میکند و به جاودانگی بیولوژیکی میرسد.
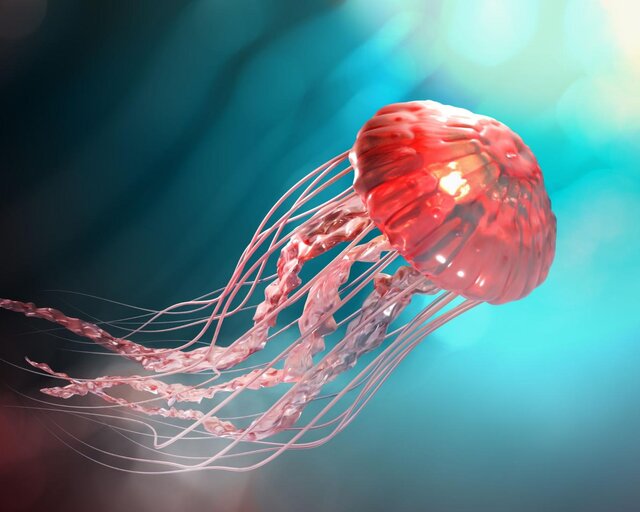
با وجود این، ترمیم DNA تنها راهبرد افزایش طول عمر نیست که انسان میتواند از حیوانات بیاموزد. پژوهشی که پیشتر انجام شد، نشان داد یک عروس دریایی کوچک اقیانوس آرام از حیواناتی است که میتوانند اعضای ازدسترفته بدن را دوباره پرورش دهند و دانشمندان دقیقا میدانند چگونه این کار را انجام میدهد.
«کلادونما پاسیفیکوم»(Cladonema pacificum) یک عروس دریایی به اندازه ناخن است که شاخک ازدسترفته را در عرض سه روز دوباره پرورش میدهد.
پژوهشگران «دانشگاه توهوکو»(Tohoku University) و «دانشگاه توکیو»(UTokyo) تصمیم گرفتند تا بفهمند که دقیقا چه اتفاقی برای سلولهای درون شاخک عروس دریایی در حین ترمیم رخ میدهد. این گروه پژوهشی دریافتند سلولهای شاخک طبیعی در محل آسیبدیده از کمک سلولهای بنیادی برخوردار میشوند که به طور ویژه برای ترمیم کردن اندام تکامل یافتهاند.
عروس دریایی نامیرا تنها نوعی است که در مراحل پس از تولید مثل، پتانسیل جوانسازی خود را تا ۱۰۰ درصد حفظ میکند و به جاودانگی بیولوژیکی میرسد.دانشمندان میگویند این سلولهای قابل توجه ممکن است کلید دستیابی به تواناییهای ترمیم اندام در انسان باشند و به پیشرفت پژوهشهای ضد پیری و افزایش طول عمر کمک کنند.
با افزایش تلاشها برای بهبود درک پیرامون علل بیولوژیکی پیری، امید است که انسانها بتوانند طول عمر خود را افزایش دهند؛ یعنی تعداد سالهایی را که در سلامت خوب زندگی میکنند، بالا ببرند.
کیگان گفت: بدن ما با افزایش سن دچار تغییرات بیولوژیکی زیادی میشود، اما واقعا مشخص نیست که کدام یک از آنها پیامدهای پیری هستند و کدام یک عامل آن به شمار میروند.
یک تغییر کلیدی در DNA سلولهای ما، تجمع تدریجی جهشها در DNA سلولهای ماست که در نهایت میتواند به بروز بیماری و ویژگیهای پیری منجر شود. آسیب DNA همیشه در سلولهای ما اتفاق میافتد و معمولا به دلیل اشتباهاتی است که هنگام ترمیم یا کپیDNA هنگام تکثیر سلولها رخ میدهند.
کیگان ادامه داد: همه گونههایی که ما بررسی کردهایم، با تعداد مشابهی از جهشهای DNA به پایان زندگی خود میرسند؛ از موشهایی که حدود سه سال عمر میکنند گرفته تا انسانهایی که عمر آنها حدود ۸۰ سال است. این نشان میدهد یک محدودیت تکاملی برای تعداد جهشهایی وجود دارد که یک ارگانیسم میتواند جمع کند.
کیگان و گروهش باور دارند که با انتقال نتایج به دست آمده از حیوانات مورد بررسی به انسان ممکن است بتوان به کلید افزایش طول عمر دست یافت.
هدف این پژوهشها یافتن راهی برای توانمند ساختن انسانها در زندگی کردن برای همیشه نیست، بلکه بهبود بخشیدن آن قسمت از زندگی ماست که سالم میگذرد. ما میدانیم که سن تقویمی ما با سن بیولوژیکی ما یکسان نیست و انتخابهای درست سبک زندگی مانند اجتناب از سیگار کشیدن و نوشیدن الکل، حفظ یک رژیم غذایی خوب و ورزش منظم حتی ممکن است سن بیولوژیکی ما را افزایش ندهند. شاید مداخلات پزشکی بتوانند اثرات ضد پیری قویتری را امکانپذیر کنند.
کلید افزایش طول عمر و شارژ سلولهای قاتل سرطان
هدف بسیاری از دانشمندان، کاهش دادن خطر بازگشت سرطان، افزایش سلولهای قاتل سرطان و کشف پتانسیل افزایش طول عمر انسان است. در میان گامهای قابل توجهی که در چند دهه گذشته برای افزایش طول عمر انسان سالم برداشته شدهاند، یک پیشرفت و نقطه عطف بسیار مهم وجود دارد که مربوط به یکی از پژوهشهای سال گذشته است.
دانشمندان «دانشگاه پزشکی تایپه»(TMU) در تایوان، یک اصلاح ژنتیکی را در موشها انجام دادند که میتواند سلولهای قاتل سرطان را بین دو تا هفت برابر قوی کند و طول عمر آنها را تا ۲۰ درصد افزایش دهد.
این گروه پژوهشی برای تقویت کردن نتایج حاصل از پژوهش پیشین خود، نتایج خارقالعادهای را که در موشهای معمولی از طریق پیوند سلولهای بنیادی خون مشاهده شده بود، تکرار کردند.
«چه کان جیمز شن»(Che-Kun James Shen) پژوهشگر ارشد این پروژه معتقد است که یافتههای آنها میتوانند پیامدهای عمیقی را برای سلامتی انسان داشته باشند. شن گفت: یافتههای جدید بسیار مهم هستند. ما امیدواریم که آنها را در آینده نزدیک اعمال کنیم و فکر میکنم اگر این کار موثر باشد، احتمالا سال آینده میتوان آزمایشهای بالینی آنها را آغاز کرد.
پژوهشگران ابتدا یک آمینواسید را شناسایی کردند. این آمینواسید، پروتئینی به نام «KLF1» بود که وقتی اصلاح شد، همه ویژگیهای سالم دوران جوانی را حفظ کرد. شن گفت: این ویژگیها شامل عملکرد حرکتی بهتر، بهبود یادگیری و حافظه و همچنین، بهبود سلولهای قاتل سرطان بود. موهای این موشها نیز بسیار تیرهتر و براقتر شد. یکی از علائم مهم پیری، فیبروزاست که به طور قابل توجهی کاهش یافت.
یافتهها نشان میدهند که این گروه پژوهشی اکنون موفق شدهاند فواید KLF1 را که نقش مهمی در رونویسی ژنهای انواع گوناگون سلولهای خونی بر عهده دارد، به لطف پیوند سلولهای بنیادی به موشهای غیرجهشیافته منتقل کنند. پیوند سلولهای بنیادی، یک روش درمانی استاندارد برای انواع خاصی از سرطانهای خون است. با تکیه بر این پیشرفت اولیه، شن و گروهش امیدوارند که با اصلاح ژنتیکی سلولهای بنیادی انسانی به کمک KLF1 بتوانند خطر ظهور مجدد سرطان را کاهش دهند و سلولهای قاتل سرطان را قوی کنند.
اگرچه از بین بردن سرطان یک چشمانداز امیدوارکننده است اما مداخله ژنتیکی گروه شن میتواند پتانسیل افزایش طول عمر انسان را نیز داشته باشد.
پژوهشگران پیشتر انواع ژنتیکی بسیاری را شناسایی کرده بودند که طول عمر موشها را افزایش میدهند. با وجود این، بخش قابل توجهی از این گونهها صرفا از موشهای ماده بهره میبردند و هیچ روش شناختهشدهای برای انتقال مزایا از موشهای جهشیافته به موشهای عادی وجود نداشت.
آزمایشهای انجامشده با KLF1 هنگام بررسی پسزمینههای ژنتیکی موشها موفقیتآمیز بودهاند و نشان میدهند هیچ پیشزمینه ژنتیکی خاصی بر نتایج تأثیر نداشته است. مزایای این پژوهش میتواند جهانی باشد و تأثیر گستردهتری را نشان دهد.
شن گفت: من فکر میکنم این روش احتمالا روی انسانها نیز کارآیی خواهد داشت. اگر این روش موفقیتآمیز باشد، دیگر نیازی به پیوند کامل مغز استخوان وجود ندارد و تنها یک جایگزینی جزئی ۳۰ یا ۲۰ درصدی برای مقاوم کردن موش به سرطان کافی است.
افزایش توانایی از بین بردن سرطان در موشهای جهشیافته، به دلیل تغییرات بیولوژیکی گوناگونی است که پس از دستکاری ژن رخ میدهند. پژوهشگران دریافتند که توانایی سلولهای قاتل سرطان مانند سلولهای T و سلولهای کشنده طبیعی حامل جایگزین آمینواسید، همگی توانایی بالاتری را در کشتن سلولهای سرطانی دارند که بین دو تا هفت برابر بیشتر از موشهای نوع وحشی است.
وقتی گروه شن متوجه شدند که اصلاح ژنتیکی آمینواسید فقط در سلولهای خونی بیان میشود، تلاش کردند تا انواع خاصی از سلولهای خونی را از موشهای جهشیافته به موشهای وحشی تزریق کنند و این کار، نتایج امیدوارکنندهای داشت.
شن امیدوار است که رویای استفاده کردن از این روش در انسان به زودی به واقعیت تبدیل شود. وی افزود: من فکر میکنم از نظر اخلاقی باید مراقب استفاده کردن از این روش باشیم اما در تلاش هستیم تا آن را انجام دهیم.
این پژوهش در مجله «Cold Spring Harbor Protocols» به چاپ رسید.

